ОСОБЕННОСТИ ВОДОРОДНОГО ИЗНАШИВАНИЯ ДЕРЕВООБРАБАТЫВАЮЩЕГО ОБОРУДОВАНИЯ
Прозоров Я.С. (БГИТА, г. Брянск, РФ)
This article is devoted to the hydrogen wear of woodworking equipment. The main sources of oxygen in the process of steel-wood’s friction are identified. The brief overview of the theories of hydrogen wear is shown.
Одной из причин износа рабочих поверхностей деталей тяжелых деревоперерабатывающих станков является насыщение в результате различных процессов и действия окружающей среды такими газами, как водород, кислород, азот и др. Водород является самым агрессивным к металлам из газов, поэтому наводороживание представляет особую опасность [1].
Установлено четыре основных источника наводороживание металлов[2,3]:
· «Биографический» водород;
· Водород, присутствующий в качестве одного из компонентов газовой фазы;
· Водород, присутствующий в водном растворе в виде ионов H+ ;
· Водород, выделяющийся при химических реакциях, происходящих в зоне трения.
«Биографический» водород — водород, содержащийся в материале деталей и накопленный при их изготовлении. Содержание водорода в готовой стали после выпуска составляет 2-10 см3/100 г. Согласно современным представлениям, источником водорода в мартеновском процессе являются шихтовые материалы (металлические и неметаллические), ферросплавы, шлам и газовая атмосфера печи;в доменном производстве - влага дутья; активное наводороживание изделий происходит при фосфатировании, азотировании и нанесении гальванических покрытий [4,5].
При деструкции древесины выделяется незначительное количество газообразного водорода H2. Источником его образования, а также ряда других газов, может быть частичный гидролиз полисахаридов древесины за счет паров воды и образующихся органических кислот при низкотемпературном разложении в некоторых условиях трения, преимущественно же при переработке сплавной древесины и древесины с длительным хранением и неправильным режимом сушки. При определенных условиях молекулы газообразного водорода адсорбируются на поверхности металла, диссоциируют на ионы и проникают в металл [6, 1]. Водород в виде ионов H+ всегда присутствует в водном растворе, очевидно его наличие в слабокислом древесном соке[6].
Важную роль в процессе наводороживания играет экзоэлектронная эмиссия на ювенильной поверхности металла, которая приводит к тому, что электроны сольватируются на молекулах воды (или других водородсодержащих материалах) и разлагают их на кислород и водород благодаря туннельному эффекту. Возникновение туннельного эффекта связано с квантовыми свойствами частиц, с тем что их движение имеет волновой характер. Благодаря этому эффекту химическая энергия, необходимая для протекания некоторых реакций (в том числе и выделения водорода), снижается на порядки.
Эмитированные из металла при трении электроны имеют первоначально избыточную энергию, которую они быстро теряют путем столкновения с молекулами воды, а затем гидратируются или вступают в химическую реакцию с присутствующими акцепторами. В гидратированном состоянии электрон существует только одну миллисекунду, после чего молекула воды распадается на водород и гидроксильный ион:
е + Н2О → ОН + Н
Обратная реакция практически никогда не идет самопроизвольно. Из большого числа окислительно-восстановительных реакций, идущих при трении различных материалов с выделением водорода, приведенная выше является наиболее производительной [5].
Кроме того, в хемосорбированных молекулах воды, находящихся в состоянии координационной связи с поверхностью окислов, в результате деформации происходит ослабление связей ОН. При этом молекулы воды протонизируются, а при повышенной температуре они даже могут потерять протон и превратиться в ОН-группы. Протонизация молекулы воды повышает ее кислотность. Адсорбированные по координационному механизму протонизированные молекулы воды являются новыми центрами дальнейшей адсорбции воды по механизму образования водородных связей [7].
В результате диссоциации воды, кислот и некоторых других органических соединений на активных центрах дорожек трения, адсорбирующиеся ионы водорода скапливаются в местах выхода на поверхность дислокаций, межфазовых границ и неупорядоченных образований и частично молялизируются. Соотношение молекул водорода и ионов может составлять приблизительно 2 : 1 [7].
Наводороживание металлической поверхности деталей узлов трения стружечного станка может происходить не только за счет действия ионов водорода, выделяющегося при диссоциации различных веществ, но и в результате химических реакций, в которых принимают участие компоненты древесины и продукты разложения древесины (органические кислоты, углеводороды, спирты, альдегиды и др.) в процессе фрикционного контакта. Экспериментальные исследования пары трения «древесина-сталь» выявили следующий состав образовавшихся неконденсировавшихся газов, %: H2 -4.2...6, CH4-2, CO – 70...72, CO2- 20 [8].
Образование водорода может происходить в результате непосредственного химического взаимодействия воды с активированным металлом поверхности. Химическую сущность процессов можно выразить такими схемами:
Fe +
2H20->Fe(OH)2 + H2
Fe + 2Н+—> Fe2++ Н2
Следствием фрикционного взаимодействия стали с древесиной является образование углеродосодержащих газов СО, СО2, CH4 , сопровождающееся обезуглероживанием поверхности узлов трения стружечных станков и выделением газообразного водорода. углерода в образце. При обезуглероживании стали учитывая, что углерод связан в карбиды, происходят реакции окисления:
Fe3C
+ О2 -> 3Fe + CO2
Fe3C + CO2-> 3Fe + 2CO
Fe3C + H20->3Fe + CО + Н2
Процесс обезуглероживания приповерхностных слоев стали обусловлен превышением скорости процесса обезуглероживания над скоростью процесса окисления железа. В результате диффузии углерода из прилегающего поверхностного слоя к реакционной зоне более или менее толстый слой металла постепенно обедняется углеродом вплоть до полного его отсутствия, то есть образования слоя чистого феррита.
Обезуглероживание приводит к снижению как механических, так и реологических свойств стали, определяемых механизмами внутреннего трения. Уменьшение количества атомов углерода в твердом растворе (обезуглероживание) будет способствовать снижению демпфирующих свойств поверхности трения и повышению износа. Кроме того, свежеобразованная в процессе трения гидроокись железа может адсорбировать растворенную в воде двуокись углерода, что будет способствовать интенсификации коррозионного процесса под слоем вторичных структур [7].
При повышенных температурах могут протекать химические реакции, основанные на термическом разложении углеводородов или на процессах конверсии углеводородов и окиси углерода, в результате чего образуется водород.
CH4+H2O->CO + 3H2
CO+H2O->CO2+H2
C2H2->2C+H2
Водородное изнашивание как один из механизмов изнашивания поверхностей при трении установлен относительно недавно и заслужило пристальное внимание научного сообщества. Водородное изнашивание возникает в результате кооперативного (синергетического) взаимодействия поверхностных явлений: экзоэмиссии, адсорбции и трибодеструкции, которые приводят к выделению водорода. Далее происходит поглощение водорода сталью путем его адсорбции и хемосорбции; концентрирование водорода в поверхностном слое преимущественно по границам зерен и в слое, деформируемом при трении приблизительно на 20-200 мкм и более, и разрушение поверхностного слоя металла на глубину до 0,1 - 0,5 мм [5].
Существует
ряд особенностей взаимодействия водорода со сталью,
связанных с характером внешнего воздействия и двумя формами существования водорода
в металле.
Первая диффузионно-активная форма - водород в виде иона pacтворен в решетке металла и вторая - молекулярная форма, здесь водород находится в молекулярном состоянии в дефектах кристаллической решетки. Окклюзия водорода в металл возможна для обеих форм.
Диффузионно-активная форма при растворении обратима и достигает равновесного значения концентрации для данных условий. Молекулярная форма оказывает охрупчивающее действие на сталь и некоторые другие металлы. Переход от растворенной формы к молекулярной зависит от дефектности стали, температуры и особенно сильно от процесса деформирования. Предельная концентрация молекулярной формы зависит от дефектности металла и может достигать пороговой концентрации, вызывающей разрушение.
Для анализа способности металла к адсорбции и абсорбции водорода используется понятие «гидридофильность», которое означает способность поверхностного слоя концентрировать в процессе трения повышенное количество водорода в ограниченном объеме под действием градиентов температуры, направленных но нормали к поверхности трения и градиентов напряжений, порожденных контактными давлениями, а также концентрационных градиента, магнитных и электрических полей. Величиной этих градиентов и областью их локализации определяется гидридофильная зона и, следовательно, степень наводороженности металла [5, 3].
Абсорбированный металлом водород может в нем находиться в различных состояниях: образовывать с металлом твердые растворы, сегрегироваться на несовершенствах кристаллической решетки, абсорбироваться на микронесплошностях и скапливаться в них в молекулярной форме, вступать во взаимодействие с металлом и вторичными фазами, то есть образовывать гидриды[3, 9].
Несмотря на большой интерес научного сообщества к водородному изнашиванию и множество посвященных этой теме работ, вопрос о его механизме является предметом острых споров исследователей в теоретическом и экспериментальном аспекте. Среди многочисленных теорий, объясняющих водородное изнашивание, можно выделить три наиболее часто привлекаемые при анализе экспериментальных данных — теорию внутреннего давления, теорию декогезии, теорию внутренней адсорбции, теория повышенного давления гидридов. Эти механизмы в значительной мере перекрываются, и, кроме того, предполагается, что может существовать и ряд других [4, 3].
Теория внутреннего давления возникла при наблюдении за образованием водородных вздутий при введении в сталь газообразного водорода. Очень высокое давление газообразного водорода, создающееся во внутренних микротрещинах и порах, вызывает пластическую деформацию или разрушение по плоскостям спайности и коалесценцию микротрещин и пор (см. рис.1).
Эта теория имеет теоретическое обоснование и получила экспериментальное подтверждение, но все же она не согласуется с достаточно большим числом феноменологических зависимостей. В частности, с ее помощью трудно объяснить растрескивание высокопрочных сталей под действием газообразного водорода при давлении 0,1 МПа и меньше, а также изменение характера разрушения от вязкого к хрупкому при наличии в стали газообразного водорода. Дальнейшим развитием этой теории послужило предположение, что движущиеся дислокации в стали служат транспортом атомов водорода. Водород, переносимый таким образом, движется быстрее и на большие расстояния, чем это может быть мотивировано с позиций диффузии только градиентами концентрации. Указанный вариант теории давления пытается растолковать наличие участков локального пересыщения водородом в условиях напряженного состояния, а также объяснить температурную зависимость водородной хрупкости, инкубационный период образования флокенов и их отсутствие в низкоуглеистых сталях. Теория давления пытается разъяснить противоречия с термодинамическими представлениями о создании высокого давления во внутренних микропорах.
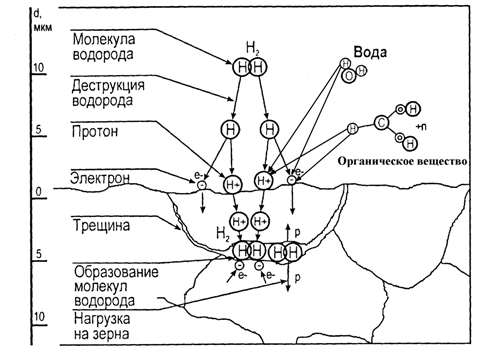
Рисунок 1- Механизм водородного изнашивания поверхности трения согласно теории внутреннего давления
Ряд авторов, однако, сомневается в возможности создания внутреннего давления из-за аннигиляции дислокаций, несущих водород, при пересечении с микропорой, поскольку было доказано, что кинетическое пересыщение, которое образуется при аннигиляции переносящих водород дислокаций, во всех реальных ситуациях невелико. Относительно водорода движущимися дислокациями указывается, что какой бы значимостью ни обладал такой перенос в кинетике распространения трещины, это не относится к проблемам механизма, посредством которого водород вызывает собственно охрупчивание стали.
В отличие от
теории молекулярного давления теория декогезии
предполагает, что растворенный водород при высоких концентрациях понижает максимальную
силу когезии между атомами вещества в кристаллической решетке, по границам
зерен и в поверхностях. Разрушение связей происходит, когда локальное
напряжение оказывается равным сниженной за счет водорода величине когезии.
Необходимые для разрушения локальные напряжения могут существовать
непосредственно в вершине трещины, а также в местах скопления дислокаций,
пересечений полос скольжения, областях пластической деформации. Теорией
декогезии можно объяснить прерывистость разрушения образцов, что обнаруживается
при измерении электросопротивления нагружаемого образца, а также существование
критической концентрации водорода. Теория декогезии противоречит некоторым
фактам об упрочнении сил связи в металле при введении водорода. Однако,
согласно ряду исследований, декогезия является преобладающим механизмом
охрупчивания высоколегированных сталей водородом, и данная модель наиболее
корректна в настоящее время. Теория декогезии имеет количественную оценку,
однако слабым звеном модели декогезии при переходе от микроскопических к
макроскопическим эффектам является необходимость определения связи между
макроскопически установленным параметрами интенсивности напряжений и
максимальными напряжениями в локализованной области (устье трещины).
Теория адсорбции связывает водородное изнашивание с понижением поверхностной энергии металла в результате адсорбции водорода и с уменьшением сил, необходимых для развития трещин. В этом случае водород действует как поверхностно-активное вещество, которое адсорбируясь на поверхности микротрещин и других дефектах, в особенности у острых вершин, существенно понижает механическую прочность твердых тел в процессе их деформации.
Согласно современным исследованиям, при адсорбции водорода на поверхности образовавшейся трещины поверхностная энергия снижается примерно на 75%, а касательное напряжение, необходимое для слияния дислокаций соответственно уменьшается примерно на половину [10].
Некоторые исследователи полагают, что предположение о понижении разрушающих напряжений из-за водорода нежизнеспособно, так как в присутствии других газов — кислорода, азота и паров воды, которые адсорбируются на чистых поверхностях даже более сильно, чем водород, разрушение не происходит. С другой стороны, рассмотрение энергетического баланса в процессе разрушения действительно подтверждает предположение о том, что разрушающее напряжение смогло бы уменьшаться, если водород мог бы снижать энергию образования двух поверхностей вследствие уменьшения сил сцепления между атомами. Таким образом, поскольку поверхностная энергия и энергия сцепления твердого тела тесно связаны, механизмы декогезии и адсорбционный в этой части объединяются. Возможные механизмы водородного изнашивания деталей узлов трения деревоперерабатывающих машин схематично изображены на рис.2 .
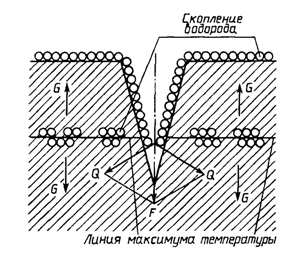
Рисунок 2 - Схема наводораживания и разрушения поверхностного слоя ножевого вала: F-давления адсорбционного слоя; Q-расклинивающие силы; G-напряжение в местах локальной концентрации водорода
Кроме того, при высоких температурах возможно не только кислородное, но и водородное обезуглероживание поверхности вала. При наводороживании стали свободный водород вступает в реакцию гидрирования с карбидами Fe3С. Вследствие этой реакции, начинающейся при температуре 240...330 oС, происходит превращение цементита Fe3С в мелкодисперсный феррит с образованием метана, который скапливается в дефектных местах границ зерен (см. рис.3).
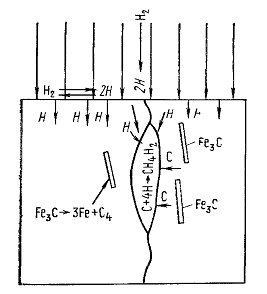
Рисунок 3- Схема процесса водородного обезуглероживания стали
В результате уменьшения концентрации карбидов в стали ухудшаются многие ее характеристики, в том числе и износостойкость. Образовавшийся метан не способен диффундировать через решетку металла, поэтому образует раковины внутри металла, что приводит к его растрескиванию[11].
Fe3C + 2Н2 -> 3Fe + СН4
Анализ всех трибохимических реакций, приводящих к обезуглероживанию образцов показывает, что их массовая доля в износе, в зависимости от рН среды и содержания кислорода, колеблется в пределах от 0,9 до нескольких процентов. Однако роль обезуглероживания в активации процессов изнашивания может быть не менее значительна, чем окисление основы - железа, поскольку уменьшение содержания в металле углерода приводит к снижению его как прочностных, так и реологических свойств, что будет способствовать падению износостойкости узла трения[8].
Литература
1. Петренко, Н.М. Повышение стойкости дереворежущего инструмента технологическими методами[Текст]:дис. … канд.тех.наук / Н.М.Петренко. - Брянск, 1984.-198 с.
2. Присевок А.Ф., Беляев Г.Я. Технология формирования газотермических водородостойких покрытий:[монография].-изд. 2е, перераб. и доп.- Минск:Технопринт, 2003.-240 с.
3. Трибохимия водородного износа [Текст]: монография / Е. А. Лукашев, М. Е. Ставровский, А. В. Олейник, В. М. Юдин, С. Г. Емельянов. - Курск : КурскГТУ, 2007. - 279 с/
4. Касаткин, Г.Н. Водород в конструкционных сталях. / Г.Н. Касаткин - М: Интермет Инжиниринг, 2003. - 336 с: ил.
5. Гаркунов, Д.Н. Триботехника (износ и безысносность): Учебник.-4-е изд., перераб. и доп./ Д.Н. Гаркунов – М.: Издательство МСХА, 2001.-616 с.:
6. Моисеев, А.В. Износостойкость дереворежущего инструмента./А.В. Моисеев. М.:Лесн.пром-сть, 1981.-112 с
7. Шевеля, В.В. Трибохимия и реология износостойкости: [Монография] / В.В. Шевеля. В.П. Олександренко. -Хмельницкий: ХНУ, 2006. 278 с.
8. Памфилов Е.А.,Петренко М.Н. К вопросу о механизме изнашивания дереворежущего инструмента. Изв.вузов.лесной журнал, 1978 г. №3, стр.148-150
9. Сорокин, Г.М. Коррозионно-механическое изнашивание сталей и сплавов /Г.М. Сорокин, А.П. Ефремов, Л.С. Саакян - М.: Нефть и газ, 2002, 424 с.
10. Максимчук, В.П. Водородное растрескивание высокопрочных сталей после нанесения гальвано-химических покрытий / В.П. Максимчук, С.П. Половников — М.: Энергоатомиздат, 2002 - 320 с. - ил.
11. Шрейдер, А.В. Влияние водорода на нефтяное и химическое оборудование/ А.В. Шрейдер, И.С.Шпарбер, Ю.И.Арчаков. - М.:Машиностроение,1976. – 144 с.